《化学平衡常数》福建西山学校高中部高二化学优秀教案
2013-12-16 18:21:49 来源: 点击:
| 课题(三) | 化学平衡常数 | |||
| 主稿:郭伟军 | 审核:任丽丽 | 日期:13年 月 日 星期 | ||
| 知识与技能: |
1、知道化学平衡常数的意义及表示方法;
2、能运用化学平衡常数进行简单的计算。
|
|||
| 过程与方法: | 通过列表计算,总结出化学平衡状态的有关方法和规律。 | |||
| 情感价值观 | 学会从定量的角度研究化学反应的限度问题。 | |||
| 教学重点: | 知道化学平衡常数的意义及表示方法 | |||
| 教学难点 | 能运用化学平衡常数进行简单的计算 | |||
| 教学过程: | 备注: | |||
| 【新课引入】 【教师】在前面的学习中,我们知道,化学平衡状态是在给定条件下可逆反应进行的最大限度,此时反应物有最大转化率。那么,当达到化学平衡时,究竟有多少反应物转化成了生成物?平衡体系中各物质的浓度之间有没有一定的关系呢?请大家完成第48页的“交流与讨论” 【学生】数据略,见表 【教师】通过计算,同学们是否发现什么规律?其中浓度的指数与化学方程式有何联系? 【学生】反应物与生成物浓度的系数次方的比值是一个定值。 【教师】很好。我们就把这个定值称为化学平衡常数。 一、化学平衡常数 1、定义:对于可逆反应aA + bB  cC +dD (四种物质都是气体) cC +dD (四种物质都是气体)在一定温度下,无论反应物的起始浓度如何,反应达到平衡状态后,将各物质的浓度代入以下表达式,得到的结果是一个定值,我们把这个常数称作化学平衡常数。 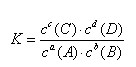 【教师】认真阅读教材中有关化学平衡常数的定义,并阅读分析表2-8和表2-9,总结可逆反应平衡常数的使用条件和书写平衡常数表达式的注意事项。 2、平衡常数表达式的书写注意点 (1)与化学方程式中化学计量数有关; (2)固体、纯液体和水的浓度不必写出; (3)平衡常数随温度的变化而变化,在使用平衡常数时应注明温度; (4)浓度是指反应达到平衡时的浓度。 【教师】那么,提出化学平衡常数概念有什么意义呢? 【学生】分析数据,找出规律:从平衡常数数值的大小可以判断反应进行的程度。K值越大,说明反应进行得越完全;K值越小,说明反应进行得越不完全。 【思考】如果给出一定温度时某个可逆反应的平衡常数,能否通过其他一些数据的测定,判断该反应是否达到化学平衡状态呢? 【引导】我们可以通过测定某一时刻体系中各物质的浓度,然后假设反应已经达到平衡,计算出平衡常数,与给定的平衡常数比较。如果相等,则假设成立,也就是说反应已达到平衡;如果不相等,则没有达到平衡。 【教师】那么,除了化学平衡常数,还可以用什么来表示化学反应进行的限度呢? 二、平衡转化率 1、某一反应物的转化率等于该物质在反应中已转化的量与反应前该物质总量的比值。 2、表达式:略,见课本 3、能表示在一定温度和一定起始浓度下反应进行的限度。 【教师】最后,大家进行小结,化学平衡常数与平衡转化率有何异同点? 【练习】课本第50页问题解决 小结: 作业:课本50面的问题解决做作业本上 |
||||
上一篇:《化学平衡状态》福建西山学校高中部高二化学优秀教案
下一篇:《物质的量在化学反应方程式中的应用》福建西山学校高中部高一化学优秀教案
 全国统一免费咨询热线:400-66-52373(欢迎来电咨询!)
全国统一免费咨询热线:400-66-52373(欢迎来电咨询!)